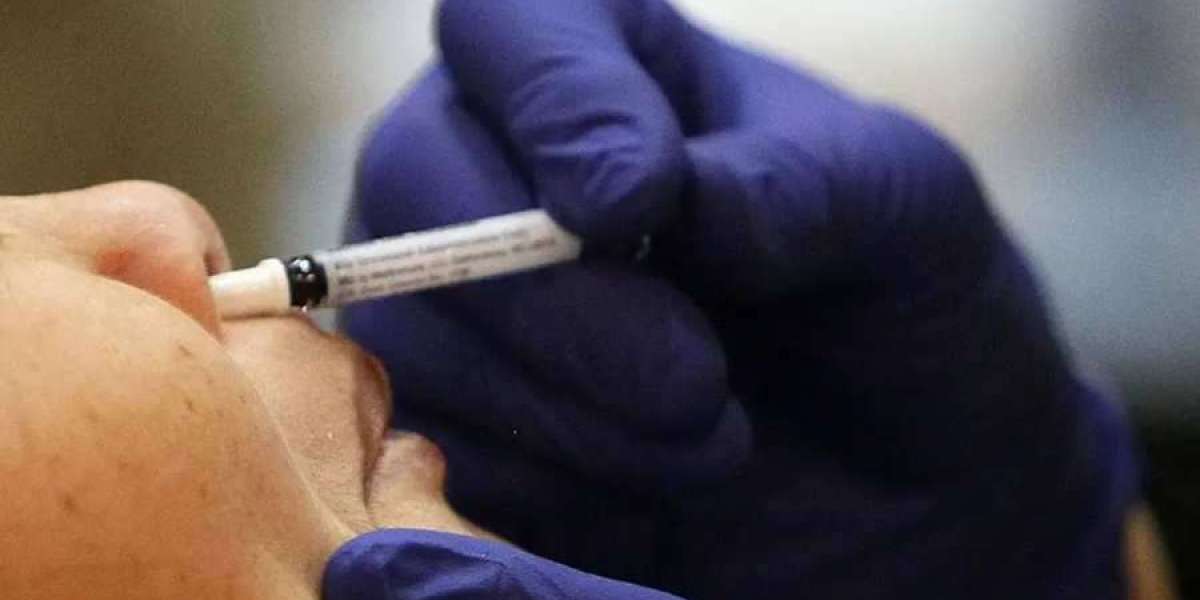
Il vaccino FluMist di AstraZeneca ha ottenuto l'approvazione della FDA verso la fine della scorsa settimana per la somministrazione a domicilio, diventando così il primo vaccino antinfluenzale "da asporto" che non necessita di essere somministrato da un operatore sanitario.
I genitori possono ora somministrare ai propri figli dai 2 anni in su, a casa, un vaccino nasale contro l'influenza che la Food and Drug Administration (FDA) statunitense ha ritirato nel 2016 perché inefficace e che è stato associato a segnalazioni di decessi infantili, secondo il Vaccine Adverse Event Reporting System (VAERS).
Secondo MedPageToday, la FDA ha approvato FluMist per l'auto-somministrazione o l'assistenza di un caregiver, per persone di età compresa tra 2 e 49 anni, con prescrizione medica. Uno studio di usabilità ha determinato che le persone di età pari o superiore a 18 anni possono auto-somministrarsi il vaccino o somministrarlo a persone idonee utilizzando le istruzioni fornite.
Il vaccino, che viene spruzzato nel naso, colpisce i sottotipi A e B del virus dell'influenza, ha affermato MedPageToday.
FluMist è stato approvato per la prima volta nel 2003, ma in precedenza la sua somministrazione era consentita solo in ambito medico e farmaceutico.
In una dichiarazione, il dott. Peter Marks, Ph.D., direttore del Center for Biologics Evaluation and Research della FDA, ha affermato che FluMist "offre una nuova opzione per ricevere un vaccino antinfluenzale stagionale sicuro ed efficace, potenzialmente con maggiore praticità, flessibilità e accessibilità per individui e famiglie".
Secondo la FDA, "FluMist contiene una forma indebolita di ceppi vivi del virus influenzale".
Brian Hooker, Ph.D., direttore scientifico di Children's Health Defense, ha detto a The Defender che "non riesce a pensare a nulla di buono che potrebbe derivare da un vaccino virale vivo somministrato a casa". Ha aggiunto:
"I vaccini con virus vivi possono avere conseguenze, soprattutto sulle donne incinte e sui neonati, per i quali questo vaccino è controindicato.
I vaccini antinfluenzali in generale portano a una miriade di eventi avversi, tra cui la sindrome di Guillain-Barré, e hanno portato a un'incidenza 4,8 volte maggiore di infezioni respiratorie acute non influenzali nei bambini di età inferiore ai 5 anni. È anche chiaro che la maggior parte degli anni, il vaccino antinfluenzale fornisce una protezione minima contro l'influenza. I rischi superano di gran lunga qualsiasi beneficio in questo caso."
Il dott. Peter McCullough ha confermato le preoccupazioni relative alla diffusione, citando uno studio del 2022 che ha dimostrato la diffusione di vaccini antinfluenzali vivi attenuati.
La dottoressa Michelle Perro, pediatra, ha dichiarato al The Defender che i vaccini con virus vivi attenuati presentano “il rischio teorico di contrarre la malattia, soprattutto negli individui immunodepressi”.
La dottoressa Meryl Nass, internista, ha criticato l'efficacia del vaccino nasale. Ha detto che FluMist è stato ritirato dal mercato per diversi anni "perché si è scoperto che era inefficace: come fanno a sapere che è efficace ora?"
Secondo la dichiarazione della FDA, FluMist è stato inizialmente approvato dalla FDA nel 2003 per le persone di età compresa tra 5 e 49 anni. Nel 2007, l' agenzia ha approvato FluMist per i bambini di età compresa tra 2 e 5 anni.
Tuttavia, nel 2018, la NBC News ha riferito che FluMist era stato ritirato dal mercato statunitense nel 2016 "perché funzionava a malapena contro un comune ceppo di influenza nei bambini". La FDA non ha menzionato il ritiro del 2016 nella sua dichiarazione del 20 settembre che approvava il vaccino per l'auto-somministrazione o la somministrazione al caregiver.
Nel 2018, il comitato consultivo sulle pratiche di immunizzazione dei Centers for Disease Control and Prevention "ha votato 12-2 per aggiungere nuovamente FluMist alla combinazione di vaccini antinfluenzali che medici e cliniche possono utilizzare", ha riferito all'epoca la NBC News.
Due membri del comitato hanno affermato di essere preoccupati di "arrecare danno ai bambini e di minare ulteriormente la percezione del pubblico sulla sicurezza dei vaccini antinfluenzali se FluMist tornasse sul mercato e non funzionasse bene", ha aggiunto la NBC News.
48 decessi, 943 gravi eventi avversi collegati a FluMist:
Secondo i dati VAERS, sono stati segnalati complessivamente 11.065 eventi avversi in relazione ai prodotti FluMist, di cui 943 classificati come "gravi". Circa la metà delle segnalazioni riguardava bambini di età inferiore ai 17 anni.
I dati VAERS mostrano che 48 segnalazioni di eventi avversi hanno causato un decesso , tra cui 23 decessi di bambini di età inferiore ai 17 anni, con altri 13 decessi elencati con un'età "sconosciuta".
Uno studio di Harvard del 2010 ha rilevato che meno dell'1% di tutti gli eventi avversi vengono segnalati al VAERS.
McCullough ha detto che FluMist ha avuto una storia travagliata, soprattutto quando si tratta di bambini. "FluMist è un vaccino impopolare dal 2003. I bambini di età inferiore ai 2 anni hanno un rischio maggiore di ospedalizzazione dopo averlo assunto. Il foglietto illustrativo afferma che si deve prestare attenzione agli asmatici e a chiunque soffra di respiro sibilante".
Perro ha affermato che alcuni ingredienti di FluMist potrebbero rappresentare un rischio:
- “La sua formulazione contiene MSG [glutammato monosodico], che è spesso prodotto da lievito geneticamente modificato, per non parlare del fatto che [potrebbe] avere proprietà neuroeccitatorie per alcuni bambini a rischio.
- "La gelatina suina probabilmente conterrà glifosato e il saccarosio sarà derivato dall'HFCS [sciroppo di mais ad alto contenuto di fruttosio]. L'antibiotico gentamicina può essere allergenico e tossico per il nostro microbiota. L'EDTA [acido etilendiamminotetraacetico] è un legante metallico che può legare anche minerali benefici".
Secondo la FDA, "Gli effetti collaterali più comunemente segnalati di FluMist sono febbre oltre i 100 °F nei bambini di età compresa tra 2 e 6 anni, naso che cola e congestione nasale negli individui di età compresa tra 2 e 49 anni e mal di gola negli adulti di età compresa tra 18 e 49 anni".
Ma Perro ha sottolineato che il sito web di FluMist afferma che gli studi clinici hanno dimostrato che "i rischi di ospedalizzazione e respiro sibilante sono aumentati nei bambini di età inferiore ai 24 mesi che hanno ricevuto FluMist trivalente" e che "i bambini di età inferiore ai 5 anni con respiro sibilante ricorrente e le persone di qualsiasi età affette da asma possono essere a maggior rischio di respiro sibilante" dopo la somministrazione di FluMist.
FluMist "non è stato studiato su persone con asma grave o respiro sibilante attivo", afferma il sito web di FluMist.
"Considerando il fatto che negli Stati Uniti fino a 1 bambino su 5 potrebbe già essere stato diagnosticato con l'asma, i potenziali rischi di un'esacerbazione dell'asma e dello sviluppo di una nuova insorgenza di asma sono significativi",ha affermato Perro.
Nass si è chiesto perché FluMist non sia approvato per gli adulti di età superiore ai 49 anni.
"È efficace per le persone anziane o non è abbastanza efficace? È pericoloso per le persone anziane? Dal momento che il gruppo target del vaccino antinfluenzale ha più di 65 anni, perché questo vaccino viene autorizzato?",ha chiesto Nass.
Il record di sicurezza di AstraZeneca messo in discussione:
Alcune delle persone intervistate da The Defender hanno messo in dubbio i risultati ottenuti da AstraZeneca in termini di sicurezza.
"AstraZeneca ha una storia orribile, considerando che la sua offerta di vaccino contro il COVID-19 (basata su un adenovirus dello scimpanzé) ha portato a così tanti gravi eventi avversi che è stato ritirato volontariamente dal mercato dal produttore", ha affermato Hooker.
"Saremmo negligenti se non discutessimo della fusione di AstraZeneca con Novartis per creare una nuova azienda, Syngenta", ha detto Perro. "Sono stati loro a molestare il professore della UC Berkeley, il dott. Tyrone Hayes, che ha esposto gli effetti tossici di interferenza endocrina del loro pesticida, l'atrazina", ha detto Perro.
"È questa l'azienda di cui dovremmo fidarci per creare un vaccino 'da asporto' da somministrare a casa?",ha chiesto Perro.
AstraZeneca è stata oggetto di una class action nel Regno Unito, intentata da persone rimaste danneggiate dal vaccino anti-COVID-19 dell'azienda e da ricorrenti che agiscono per conto di una persona cara presumibilmente morta a causa di problemi di coagulazione del sangue indotti dal vaccino.
Perro ha affermato che i genitori dovrebbero prendere in considerazione soluzioni alternative per proteggere i propri figli dall'influenza:
- "I bambini se la cavano molto bene clinicamente quando hanno a che fare con una malattia influenzale, che deriva dalla mia cura di migliaia di bambini con l'influenza. I genitori avranno difficoltà a trovare informazioni su come prendersi cura dei loro figli quando esposti a causa della pulizia di Internet e dell'inondazione dei motori di ricerca con messaggi pro-vaccino antinfluenzale.
- “Ad esempio, ci sono spray nasali che possono essere usati quando i bambini sono esposti all'influenza e che possono ridurre al minimo i rischi, così come diete/integratori che possono rafforzare l'immunità, come le vitamine C e D. Questo tipo di educazione alla salute pubblica è quasi inesistente in una narrazione guidata dall'industria farmaceutica.”
"Poiché ogni bambino ha una probabilità di contrarre l'influenza in un dato anno molto inferiore all'1%, è più opportuno essere pronti a curare questa rara infezione piuttosto che essere disturbati da FluMist o da qualsiasi altro vaccino antinfluenzale",ha affermato McCullough.
fonte